Строй-Техника.ру
Строительные машины и оборудование, справочник
Коррозией называется разрушение металлов и сплавов под действием окружающей среды. Подавляющее большинство металлов, применяемых в технике, в различной степени подвержено коррозии.
Коррозия обычно начинается с поверхности и затем распространяется в глубину металла, вследствие чего ухудшаются его механические свойства. Среда, в которой протекают коррозионные процессы, оказывает большое влияние на их характер, в связи с чем различают два основных вида коррозии: химическую и электрохимическую.
Химическая коррозия возникает в результате воздействия на металлы жидкостей, сухих газов, которые не являются проводниками электрического тока (бензин, масла, смолы, газы и т. п.). При химической коррозии на поверхности металлов образуются пленки окислов. Такие пленки некоторых металлов (алюминий, хром, молибден) обладают высокой прочностью и предохраняют металл от разрушения. Пленки окислов железа и других черных металлов непрочны. Местные разрушения этих пленок окислов и являются причиной дальнейшего протекания коррозии, проникающей в металл на большую глубину.
Рекламные предложения на основе ваших интересов:
Дополнительные материалы по теме:
Окисление металлов при повышенных температурах с образованием на их поверхности окалины является типичным видом химической коррозии.
Электрохимическая коррозия является результатом воздействия на металлы различных электролитов — кислот, щелочей, растворов солей и воды с растворенными в ней газами и примесями. Все эти жидкости, являются хорошими проводниками тока.
Одним из наиболее распространенных видов электрохимической коррозии является атмосферная коррозия металлов, сущность которой заключается в следующем. Из физики известно, что пластинки, изготовленные из разнородных металлов и соединенные между собой, при погружении в электролит образуют гальванические пары. При этом металл, обладающий более высоким электрическим потенциалом, будет являться катодом, а металл с более низким потенциалом — анодом.
В промышленности наибольшее применение имеют сплавы, а не чистые металлы. Состав сплавов не является однородным. Например, перлитная сталь состоит из зерен феррита и цементита и других примесей, в результате чего получается множество гальванических пар, в которых зерна феррита являются катодом, а зерна цементита — анодом.
При соприкосновении с влажным воздухом на поверхности стали появляется влага в виде водяной пленки, которая является в данном случае электролитом. При. этом появляются токи, являющиеся основной причиной коррозии металла. Следовательно, электрохимическая коррозия отличается от химической тем, что при ней происходят электрохимические процессы вследствие возникновения токов.
Защита металлов от коррозии. Коррозия металлов причиняет огромные убытки народному хозяйству. Основными металлами в машиностроении и в других отраслях народного хозяйства являются черные, т. е. сталь и чугун. Они обладают слабой стойкостью против коррозии, вследствие чего выходит из строя большое количество деталей из черных металлов.
Металлические изделия защищают от коррозии различными способами: металлическим и неметаллическим покрытием, созданием на их поверхности окисных пленок и легированием металлов и сплавов.
Для защиты металлов и сплавов от коррозии неметаллическими покрытиями поверхность изделия окрашивают различными красками, покрывают лаками и пр.
Легирование металлов и сплавов осуществляют введением хрома, никеля, алюминия, кремния и других элементов, повышающих сопротивление коррозии.
—
Коррозией металлов называется их разрушение вследствие химического или электрохимического взаимодействия с коррозионной средой.
Виды коррозии. Коррозия металлов и сплавов начинается с их поверхности и постепенно распространяется в глубь материала. При этом внешний вид металлов изменяется: они теряют блеск, их поверхность становится неровной, изъеденной. Часто коррозия металлов сопровождается снижением их механической прочности, твердости и другими явлениями. Примером коррозии металлов может служить ржавление железа под воздействием влажного воздуха, в результате чего на поверхности металлов образуется бурый слой ржавчины.
В зависимости от состояния коррозионной среды, вида металла и условий их взаимодействия на поверхности металла образуются различные химические соединения, так называемые продукты коррозии. Они могут быть в виде пленок и наростов с плотной и рыхлой структурой, прочно приставших к поверхности металла или легко удаляемых с него.
Пленки, особенно если они плотные (беспористые), могут тормозить дальнейший процесс коррозии, а в некоторых случаях надежно защищать металл от разрушения. Например, пленка, образовавшаяся на алюминии при воздействии кислорода воздуха, защищает его от дальнейшей коррозии. При образовании защитной пленки металл теряет способность к химическим взаимодействиям с окружающей средой, т. е. переходит в пассивное состояние. Но достаточно удалить защитную пленку и коррозия металла начинается снова.
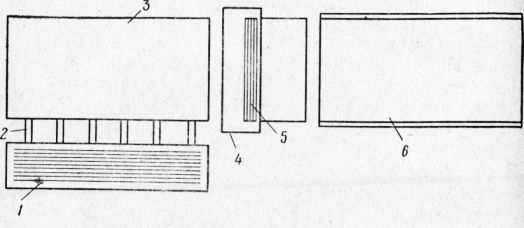
Рис. 1. Виды коррозии:
а — сплошная (равномерная) коррозия, б — местная, в — межкристал-лнтная; 1 — металл, 2, 3 — продукты коррозии, 4 — трещины
В зависимости от характера протекания коррозионного процесса, состояния коррозионной среды, природы металла и действующих на него напряжений (изгибающих, сжимающих, ударных, растягивающих) наиболее часто встречаются три вида коррозии: сплошная, местная и межкристаллитная.
Сплошная коррозия, охватывающая всю поверхность металла, подразделяется на равномерную и неравномерную.
Равномерная коррозия протекает с одинаковой скоростью по всей поверхности металла, а неравномерная протекает с неодинаковой скоростью на различных участках поверхности металла.
Равномерная коррозия происходит в большинстве случаев на открытом воздухе.
При коррозии этого вида металл разрушается равномерно по всей поверхности конструкции или аппарата. Если с поверхности металла удалить слой ржавчины, то можно увидеть, что его поверхность стала шероховатой. При более длительном воздействии воздуха углубления в металле увеличиваются.
Местная коррозия — это коррозия, охватывающая отдельные участки поверхности металла. Такая коррозия подразделяется на подповерхностную, точечную, сквозную и коррозию пятнами.
Местная коррозия возникает при наличии в металле загрязнений (шлаков и др.), внутренних напряжений, вследствие вмятин, наклепа; при грубой структуре и неоднородности поверхности металла; неравномерном действии коррозионной среды; при неравномерной аэрации поверхности металла.
Коррозия вследствие неравномерной аэрации часто возникает на тех участках металла, которые менее доступны воздействию кислорода, чем остальная поверхность. Такими участками являются царапины, раковины, заклепочные швы конструкций и т. п.
Местная коррозия на отдельных участках металла резко снижает его механическую прочность, что приводит к преждевременному разрушению оборудования и металлических конструкций, нарушению герметичности емкостей и трубопроводов.
Межкристаллитная коррозия распространяется по границам кристаллов-зерен, составляющих металл, и нарушает между ними связь. Это вызывает снижение механической прочности материала. Особенностью коррозионного разрушения этого вида является то, что коррозия распространяется глубоко внутрь металла, не изменяя внешнего вида металлической конструкции. Межкристаллитная коррозия чаще всего поражает конструкции, изготовленные из нержавеющей стали и алюминиевых сплавов. Разрушение конструкции происходит внезапно в результате резкого падения прочности металла или сплава.
Межкристаллитная коррозия обычно возникает в зоне сварных швов. Это объясняется тем, что при термической обработке нержавеющих сталей (высокохромистых) при высокой температуре — (1000—1110 °С) и последующем относительно быстром охлаждении происходят изменения состава металла по границам кристаллов за счет образования карбидов, т. е. соединений железа с углеродом, обладающих меньшей устойчивостью к коррозионным средам по сравнению с хромом.
Склонность алюминиевых сплавов к межкристаллитной коррозии объясняется образованием по границам зерен соединений менее коррозионностойких, чем основная часть зерен металла.
Часто можно наблюдать, что металл одновременно подвергнут нескольким видам коррозии. Равномерная коррозия, например, сопровождается местной и т. д.
Типы коррозии. В зависимости от вида коррозионной среды коррозия металла может происходить химическим или электрохимическим путем.
Химическая коррозия возникает при действии на металлы сухих газов при высоких температурах или жидких неэлектролитов (жидкостей, не проводящих электрический ток). К химической коррозии относится также разрушение металла кислородом сухого воздуха и другими газами (углекислым, сернистым) при отсутствии паров воды.
При химической коррозии происходит взаимодействие коррозионной среды с поверхностью металла, в результате которого продукты коррозии (пленки, окислы, окалина) образуются непосредственно на том участке поверхности металла, где происходит его разрушение.
Электрохимическая коррозия возникает при взаимодействии металла с жидкой коррозионной средой (растворами электролитов, т. е. жидкостями, проводящими электрический ток), влажными газами, расплавленными солями и щелочами. Электролитами служат растворы кислот, солей или щелочей. При электрохимической коррозии разрушение металла связано с возникновением и перетеканием электрического тока с одних участков металла на другие.
Чтобы понять сущность электрохимической коррозии, рассмотрим некоторые явления, лежащие в основе этого процесса. Если в сосуд с разбавленной серной кислотой опустить два разнородных металла, например медь и цинк, и соединить их проводником, то по нему потечет электрический ток. Полученный источник тока называется гальваническим элементом.
Возникновение электрического тока в гальваническом элементе объясняется следующим. В растворе серной кислоты (электролите) молекулы вещества распадаются на части, которые называются ионами. Ионы каждого химического вещества несут определенный химический заряд: положительный (катион) или отрицательный (анион).
При погружении цинковой пластинки в электролит между кислотой и металлом возникает взаимодействие, в результате которого цинк постепенно-переходит в раствор. При этом каждый атом цинка оставляет-на металлической пластинке два электрона, а сам становится в растворе положительным ионом.
Цинковая пластинка, обогащаясь электронами, приобретает отрицательный электрический заряд. Слой электролита, непосредственно прилегающий к пластинке, заряжается при этом положительно. Между пластинкой и раствором кислоты возникает разность потенциалов (электрических зарядов).
Освободившиеся на цинковой пластинке (аноде) электроны текут по внешнему проводнику к медной пластинке (катоду). Электрическая цепь’ замыкается через электролит, в котором ионы переносят ток. В результате работы гальванического элемента цинковая пластинка (анод) постепенно разрушается.
Электрохимическая коррозия металла напоминает постепенное растворение анода гальванического элемента.
При эксплуатации химического оборудования под действием электролита происходит разрушение металла в результате образования гальванических элементов. Например, в химическом аппарате, изготовленном из нескольких различных металлов, при действии электролита у мест сопряжения этих металлов создаются условия для возникновения гальванического элемента, в результате работы которого металл разрушается и переходит в раствор.
В отличие от обычного гальванического элемента, где электроды соединены проводником, в гальваническом элементе, возникающем при коррозии химической аппаратуры, электроды соединены между собой непосредственно.
При изготовлении металлических аппаратов и строи, тельных конструкций всегда учитывают возможность возникновения электрохимической коррозии от соединения различных металлов.
Недопустимо, например, соединять без изолирующих прокладок алюминий с медными сплавами или с нержавеющими сталями.
Причиной возникновения электрохимической коррозии в металлическом аппарате или конструкции может служить также физическая неоднородность металла. Например, коррозия часто возникает в местах расположения сварных и заклепочных швов. Это объясняется тем, что при сварке металла в результате его нагревания на сравнительно небольшом участке происходит изменение структуры металла. При действии коррозионной среды этот участок по отношению к основному металлу конструкции становится анодом и начинает разрушаться. Такой же процесс возникает, если в конструкции есть заклепочные швы: заклепки становятся анодами по отношению к основному металлу и образуют с ним гальванический элемент.
Очень часто металл разрушается в результате возникновения на его поверхности микрогальваноэлементов, что происходит из-за его химической или физической неоднородности. Например, цинк, применяемый для различных технических целей, в своем составе содержит ряд примесей различных металлов и в том числе медь. Так как-растворимость меди в цинке ограничена, то при содержании ее в цинке выше определенной нормы медь выделяется в виде отдельных мелких включений. В результате этого на поверхности цинка возникают мельчайшие, невидимые глазу гальваноэлементы, в которых катодами являются частицы меди, а анодами — цинк. При работе микроэлемента цинк переходит в электролит, что в конечном счете приводит к полному разрушению цинковой пластинки.
Обычно конструкционная сталь, из которой изготовляют химическую аппаратуру, технологические и строительные конструкции, также отличается химической неоднородностью. Эта неоднородность обусловливает низкую коррозионную стойкость стали в коррозионных средах и вызывает необходимость в осуществлении мероприятий по защите оборудования и конструкций от коррозии.
Коррозионная стойкость. Не все металлы и сплавы в одинаковой степени разрушаются коррозионными средами. Одни разрушаются быстрей, другие в тех же условиях оказываются устойчивыми к действию коррозии в течение длительного времени. Однако нет металлов совершенно не подвергающихся коррозии. Например, одним из наиболее устойчивых металлов является платина, но и она при погружении в смесь азотной и соляной кислот разрушается. Алюминий устойчив к воздействию крепкой азотной кислоты (поэтому его используют для изготовления цистерн и хранилищ под азотную кислоту), но если в алюминиевые аппараты залить соляную кислоту или щелочные растворы, то они очень быстро разрушат этот металл.
Способность металла сопротивляться коррозионному воздействию среды, называется коррозионной стойкостью. Она определяется качественно и количественно (скоростью коррозии в данных условиях, группой или баллом >по принятой шкале).
Одним из основных методов испытания металла на коррозионную стойкость является массовый метод. При испытании этим методом определяют разность массы образца металла до и после коррозии. Результаты испытаний относят к единице поверхности металла (м2, см2) и единице времени (час, сутки, год и т. д.). Таким образом, коррозионные потери могут быть выражены в г/см2-ч\ г/м2-день и т. д. Однако массовый метод не учитывает плотности металла. В результате этого при одной и той же потере массы для разных металлов уменьшение сечения металла будет (различным.
При коррозии, сосредоточенной на небольших участках металла, массовый метод неприменим. В этом случае глубину проникновения коррозии определяют с помощью специальных методов.
Для более точного определения коррозионной стойкости металла полученные данные массового метода приводят к показателю, который характеризует уменьшение толщины металла (проникновение коррозии в глубину металла), например в мм/год.
Рекламные предложения:
Главная → Справочник → Статьи → Форум
Механизация земляных работ
Механизация строительства
Механизация дорожных работ
Автоматизация строительства
→ Бетонные работы
→ Мини-тракторы
 Разделы
Разделы
Строительные машины и оборудование
→ Для специальных земляных работ
→ Дорожно-строительные машины
→ Строительное оборудование
→ Асфальтоукладчики и катки
→ Большегрузные машины
→ Строительные машины, часть 2,
→ Дорожные машины, часть 2
→ Ремонтные машины
→ Ковшовые машины
→ Автогрейдеры
→ Экскаваторы
→ Бульдозеры
→ Скреперы
→ Грейдеры
Эксплуатация строительных машин
→ Эксплуатация средств механизации
→ Эксплуатация погрузочных машин
→ Эксплуатация паровых машин
→ Эксплуатация экскаваторов
→ Эксплуатация подъемников
→ Эксплуатация кранов перегружателей
→ Эксплуатация кузовов машин
→ Крановщикам и стропальщикам
Ремонт строительных машин
Ремонт дорожных машин
Ремонт лесозаготовительных машин
Ремонт автомобилей КАмаЗ
Техническое обслуживание автомобилей
Очистка автомобилей при ремонте
Материалы и шины
Остались вопросы по теме:
"Коррозия металлов"
— воспользуйтесь поиском.
→ Машины городского хозяйства
→ Естественная история машин
→ Транспортная психология
→ Пожарные автомобили
→ Автомобили-рефрижераторы
→ Монтаж и эксплуатация лифтов
→ Тракторы